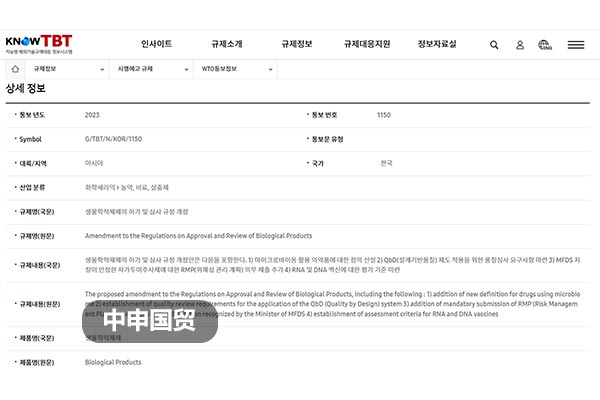
韓國修訂生物制劑等品種許可、審查規定
韓國食品藥品安全部(MFDS)于2023年6月26日,向WTO提交了G/TBT/N/KOR/1150號通知,計劃對《生物制劑等品種許可、審查規定》進行修訂,以加強國內生物制劑安全。修訂內容包括對新出現的活菌制劑等名詞的定義,適用于設計質量體系的質量審核要求,藥理作用和臨床試驗效果資料的“科學論文引用索引”范圍的擴大,變更制造方法時,改善穩定性試驗資料的提交條件的更改,MFDS認可的自行注射產品的風險管理計劃的強制性提交程序的新增,以及RNA和DNA疫苗評價標準的建立。鑒于中國是全球第二大生物制劑市場,此次修訂對我國出口企業有重要影響,企業需密切關注并適應這些變化。











 滬公網安備31011502009912號
滬公網安備31011502009912號